Novos medicamentos aprovados pela FDA em 2025
A oncologia segue como a principal área terapêutica nas aprovações da FDA em 2025, impulsionada pelo avanço de terapias direcionadas a alvos moleculares.
BLOG CIENP
Sara Tolouei, PhD; Fabiana C. V. Giusti, PhD e João B. Calixto, PhD
1/8/20264 min read
O ano de 2025 foi marcado por um volume expressivo de inovações terapêuticas aprovadas pela agência reguladora de alimentos e medicamentos dos Estados Unidos (FDA - Food and Drug Administration). Ao todo, 46 novos medicamentos inéditos receberam autorização ao longo do ano, abrangendo desde tratamentos altamente especializados para doenças raras até novas opções para condições terapêuticas comuns que impactam significativamente a qualidade de vida. Embora esse número represente uma leve redução na média dos últimos cinco anos, que passou a 48 novos medicamentos por ano, o volume de aprovações permanece substancialmente acima da média histórica, estimada em 36 novos medicamentos anuais desde 1993. A evolução anual do número de novas entidades moleculares e produtos biológicos aprovados pela FDA desde 1993 está apresentada na Figura 1.
Essas aprovações refletem o avanço contínuo da pesquisa farmacêutica, com destaque para terapias direcionadas, medicamentos biotecnológicos, pequenas moléculas inovadoras e abordagens cada vez mais personalizadas.


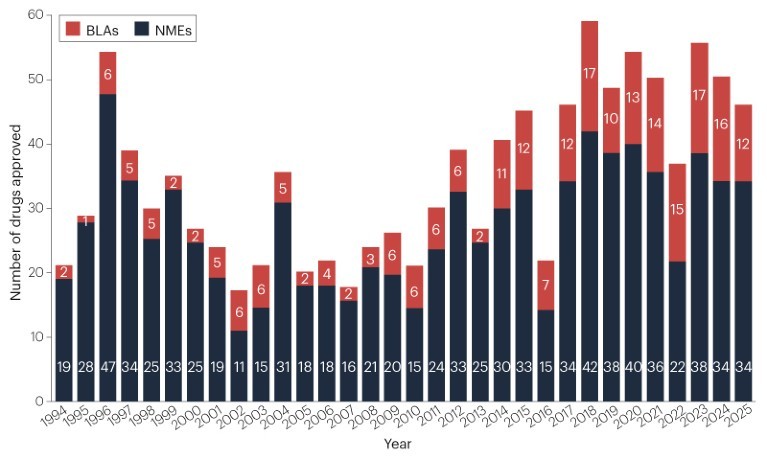
Figura 1. Evolução anual das aprovações de medicamentos pela FDA (1993-2025). Número de novas entidades moleculares (NMEs) e produtos biológicos (BLAs) aprovados pelo Center for Drug Evaluation and Research (CDER). Fonte: Mullard, 2025.
Contexto regulatório da FDA em 2025
O ano de 2025 também foi marcado por mudanças relevantes no ambiente regulatório da FDA. Alterações internas na estrutura da agência e ajustes em políticas regulatórias ocorreram em paralelo ao processo de avaliação de novos medicamentos, criando um cenário desafiador do ponto de vista institucional. Ainda assim, a FDA manteve sua atuação regulatória e avançou com iniciativas voltadas à modernização dos processos de aprovação.
Entre essas iniciativas, destacam-se a introdução de novos programas destinados a acelerar a análise de medicamentos considerados prioritários, bem como a ampliação de abordagens regulatórias alternativas para situações em que ensaios clínicos tradicionais não são factíveis. Essas mudanças refletem uma tendência de maior flexibilidade regulatória, especialmente para terapias altamente inovadoras, personalizadas ou voltadas a doenças raras.
O que caracteriza um novo medicamento
Para fins regulatórios, um medicamento é classificado como “novo” quando contém um ingrediente ativo que nunca foi previamente aprovado para uso nos Estados Unidos. Essa definição inclui tanto pequenas moléculas quanto produtos biológicos, abrangendo medicamentos com mecanismos de ação inéditos, novas classes terapêuticas ou abordagens clínicas inovadoras. Em muitos casos, esses produtos são desenvolvidos para atender necessidades médicas ainda não plenamente contempladas, como doenças raras, condições graves ou subgrupos específicos de pacientes definidos por características genéticas ou moleculares.
Principais áreas terapêuticas contempladas em 2025
As aprovações de novos medicamentos em 2025 abrangeram um amplo espectro de indicações médicas, com predomínio de áreas associadas a elevada complexidade clínica e a necessidades médicas ainda não plenamente atendidas. Destacaram-se, em especial:
Oncologia, incluindo tumores sólidos e neoplasias hematológicas, com forte presença de terapias direcionadas a alterações moleculares específicas;
Doenças raras e genéticas, refletindo o avanço de estratégias regulatórias voltadas a populações de pacientes menores e altamente especializadas;
Doenças autoimunes e inflamatórias, ampliando o arsenal terapêutico para condições crônicas de difícil controle;
Doenças cardiovasculares e metabólicas, incluindo dislipidemias e cardiomiopatias;
Doenças respiratórias, como asma eosinofílica grave e fibrose pulmonar idiopática;
Infecções bacterianas, com a introdução de novas opções terapêuticas frente a patógenos resistentes;
Condições que impactam a qualidade de vida, como dor aguda, presbiopia, olho seco, sintomas vasomotores da menopausa e náuseas associadas ao movimento.
A oncologia consolidou-se como a principal área terapêutica em 2025, respondendo por aproximadamente 35% das novas aprovações, percentual superior à média dos últimos cinco anos. Esse cenário reflete a intensificação do desenvolvimento de medicamentos baseados em alvos moleculares bem definidos, reforçando a integração entre diagnóstico de precisão e tratamento farmacológico. Além da oncologia, áreas como cardiologia e doenças alérgicas e inflamatórias também apresentaram participação relevante entre as novas aprovações, indicando uma diversificação progressiva do portfólio terapêutico para condições crônicas e de alta prevalência clínica.
Do ponto de vista tecnológico, observou-se uma predominância de medicamentos de pequenas moléculas entre os produtos aprovados pelo CDER em 2025. Destaca-se o crescimento expressivo dos inibidores de quinases, que corresponderam a cerca de um terço das novas pequenas moléculas aprovadas, evidenciando a maturidade e a expansão dessa classe farmacológica para além da oncologia. Embora anticorpos monoclonais e terapias avançadas, como terapias gênicas, continuem a desempenhar papel estratégico, especialmente no tratamento de doenças raras e condições de elevada complexidade clínica, seu número absoluto de aprovações permaneceu inferior ao das pequenas moléculas. Esses dados indicam que, apesar dos avanços em biotecnologia, as pequenas moléculas seguem como eixo central da inovação farmacêutica, em função de sua versatilidade terapêutica, robustez regulatória e potencial de maior acessibilidade aos sistemas de saúde.
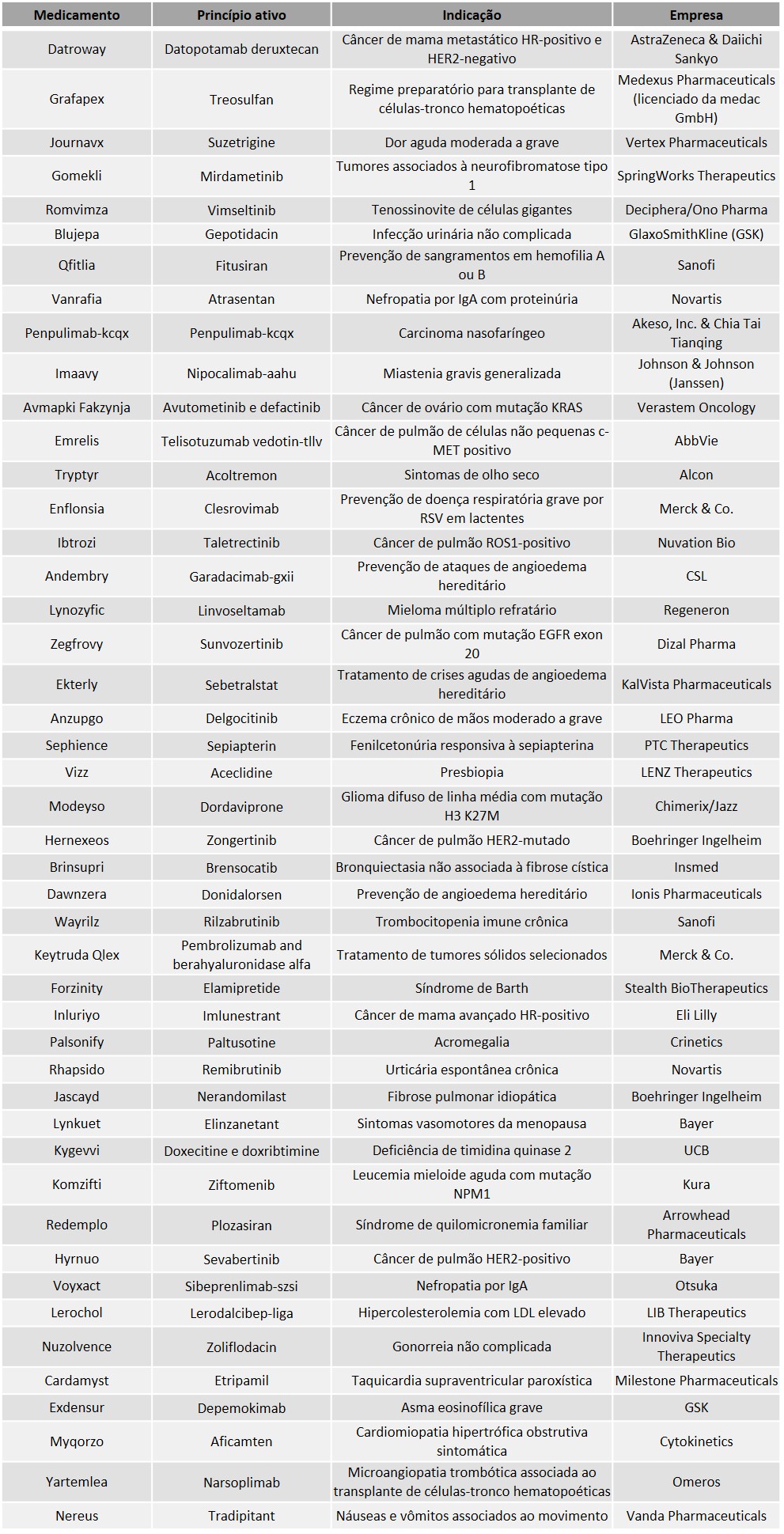
Tabela 1. Novas terapias medicamentosas aprovadas pela FDA em 2025.
Conclusão
As aprovações concedidas pela FDA ao longo de 2025 evidenciam um ambiente regulatório favorável à inovação, com destaque para medicamentos que introduzem novas abordagens terapêuticas e ampliam as possibilidades de tratamento em diferentes áreas da medicina.
No entanto, as decisões da FDA representam apenas uma parte do cenário regulatório internacional. Outras agências reguladoras, como a Agência Europeia de Medicamentos (EMA) e a Agência Reguladora de Medicamentos e Produtos de Saúde do Reino Unido (MHRA), ainda não divulgaram suas próprias listas de aprovações, que, em conjunto, permitirão uma compreensão mais ampla e integrada do panorama global de inovação farmacêutica.
Referências consultadas
Dunleavy, K. 2025 approvals: Biopharma delivered 55 new drugs, biologics. Fierce Pharma, 5 Jan. 2026. Disponível em: https://www.fiercepharma.com/pharma/2025-drug-approvals.
Mullard A. 2025 FDA approvals. Nat Rev Drug Discov. 2026 Jan 2. doi: 10.1038/d41573-026-00001-z. Epub ahead of print. PMID: 41482567.
Endereço
Av. Luiz Boiteaux Piazza, 1302 - Sapiens Parque, Cachoeira do Bom Jesus, Florianópolis, Santa Catarina, Brasil.
Segunda a sexta-feira das 08:00 às 17:00 horas.
©2024 - Centro de Inovação e Ensaios Pré-Clínicos
Mapa do site
Serviços
+55 (48) 3332-8400
contato@cienp.org.br
