Avanços e desafios na aprovação e comercialização de medicamentos para tratamento da obesidade
Com o avanço da ciência e o crescimento da prevalência da obesidade em todo o mundo, surgem novos desafios e oportunidades no desenvolvimento, aprovação e acesso a medicamentos mais eficazes. Esta edição apresenta um panorama atualizado sobre as principais inovações terapêuticas, estratégias regulatórias e barreiras econômicas envolvidas no tratamento da obesidade, além de destacar perspectivas futuras que podem transformar a forma como essa doença é abordada globalmente.
BLOG CIENP
Fabiana C. V. Giusti, PhD; Sara Tolouei, PhD e João B. Calixto, PhD
7/15/20256 min read


Avanços recentes e novas abordagens no tratamento da obesidade
A obesidade é uma doença crônica complexa que cresce em todo o mundo, elevando o risco de diabetes tipo 2, doenças cardiovasculares, câncer e problemas hepáticos, além de gerar alto impacto na saúde pública e na economia global. Estima-se que mais de 650 milhões de adultos sofram dessa condição, o que impulsiona a busca por tratamentos eficazes.
Recentemente, houve uma revolução no tratamento farmacológico da obesidade com o reposicionamento dos agonistas do GLP-1 (glucagon-like peptide-1), inicialmente criados para diabetes tipo 2. Esses medicamentos atuam em receptores no trato gastrointestinal, pâncreas e cérebro, promovendo saciedade, reduzindo o apetite e melhorando fatores metabólicos, como controle da pressão arterial e níveis lipídicos. Isso amplia sua indicação para o tratamento da obesidade, proporcionando uma abordagem integrada e eficaz.
Um avanço recente foi desenvolvimento da tirzepatida, comercializada como Mounjaro pela Eli Lilly, que age simultaneamente nos receptores GLP-1 e GIP (polipeptídeo insulinotrópico dependente de glicose). Essa ação dupla produz efeitos sinérgicos, melhorando o controle glicêmico e promovendo maior perda de peso em comparação aos agonistas de GLP-1 isolados. Um novo estudo publicado em 3 de julho de 2025 no New England Journal of Medicine reforça essa superioridade terapêutica: em 72 semanas, a tirzepatida proporcionou uma perda média de –20,2% do peso corporal, contra –13,7% com a semaglutida.
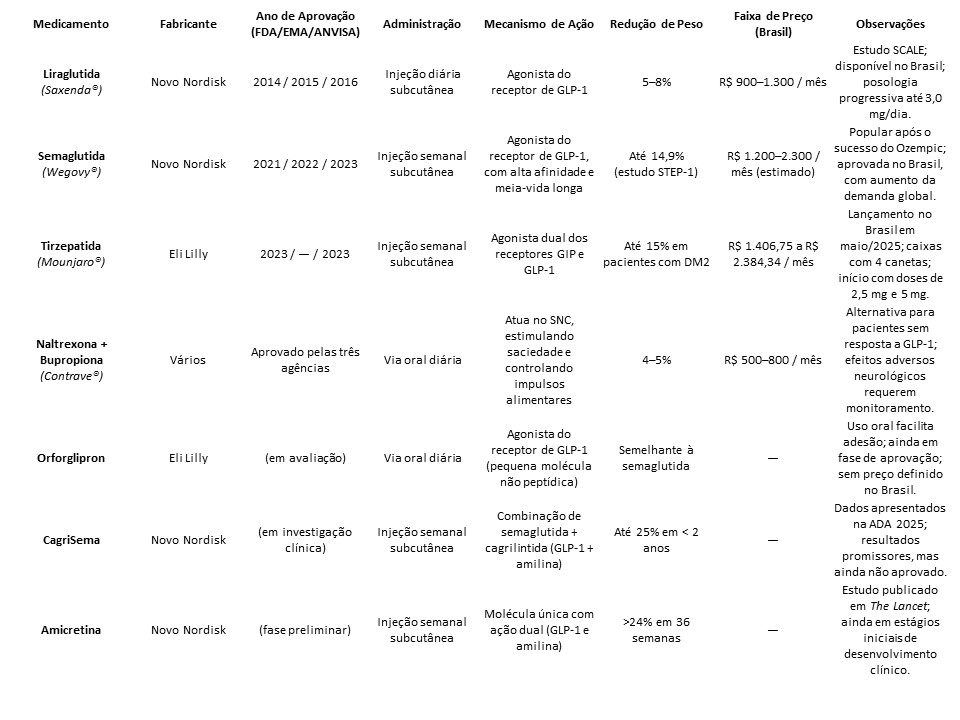
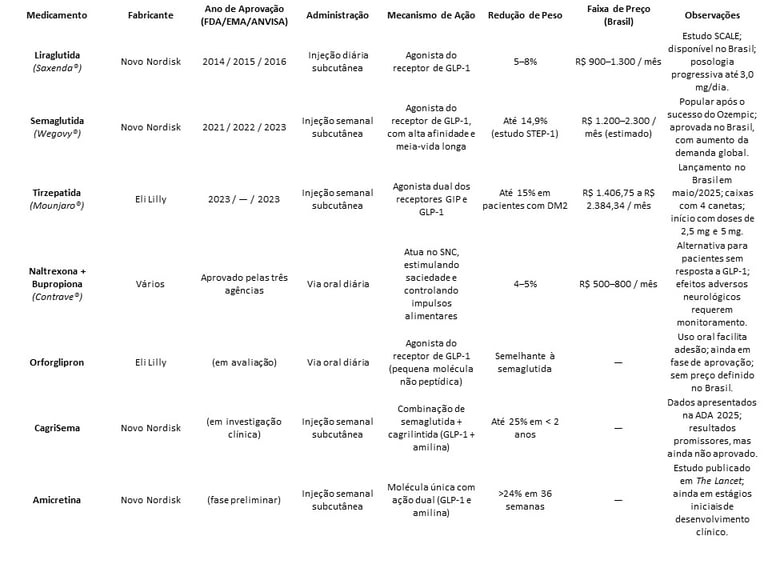
A tabela a seguir reúne os principais medicamentos aprovados ou em desenvolvimento para o tratamento da obesidade. São apresentadas informações sobre o fabricante, ano de aprovação (quando disponível), forma de administração, mecanismo de ação, eficácia na redução de peso e a faixa de preço estimada no Brasil. Essa visão comparativa ajuda a entender as diferenças entre as terapias, suas inovações e o potencial impacto clínico e econômico no cuidado com a obesidade.
Tabela 1. Medicamentos aprovados e em desenvolvimento para o tratamento da obesidade.
Cenário global e regulação: avanços e desigualdades
O mercado global de medicamentos para obesidade cresceu significativamente, atingindo cerca de US$ 100 bilhões em 2024, com projeção para US$ 150 bilhões até 2033, impulsionado pela maior demanda e avanços na cadeia de suprimentos. As empresas Novo Nordisk e Eli Lilly lideram o segmento, sendo as únicas com agonistas do receptor GLP-1 aprovados para perda de peso. Enquanto a Novo Nordisk comercializa a semaglutida sob os nomes Ozempic e Wegovy, a Eli Lilly oferece tirzepatida (Mounjaro para diabetes tipo 2 e Zepbound para obesidade). A Eli Lilly tem se destacado com crescimento projetado de 41% em 2025, superando os 25% da Novo Nordisk.
Esse avanço reflete o reposicionamento de medicamentos originalmente desenvolvidos para diabetes, como a liraglutida e a semaglutida, ampliando as opções para pacientes com obesidade. Entretanto, a obesidade ainda enfrenta desafios regulatórios e de acesso, incluindo a necessidade de comprovação de segurança a longo prazo e barreiras econômicas globais.
A China vem se posicionando no desenvolvimento da próxima geração de tratamentos orais para obesidade, com empresas como a Verdiva Bio planejando iniciar ensaios clínicos de moléculas inovadoras ainda em 2025, o que pode ampliar o acesso mundial a terapias eficazes e mais acessíveis.
Quanto à regulação, FDA (EUA), EMA (União Europeia) e ANVISA (Brasil) adotam abordagens rigorosas, refletindo suas prioridades locais. A FDA, após a retirada da sibutramina em 2010 devido a riscos cardiovasculares evidenciados em estudos como o SCOUT, exige hoje que novos medicamentos para obesidade demonstrem eficácia e segurança cardiovascular, incluindo estudos robustos de desfechos cardiovasculares. A EMA também valoriza estudos clínicos abrangentes e monitoramento pós-comercialização, avaliando cuidadosamente o risco-benefício para diferentes grupos, como idosos e pacientes com comorbidades.
No Brasil, a ANVISA avalia medicamentos considerando segurança, eficácia e custo-efetividade, dada a limitação de recursos do SUS. Atualmente, o SUS oferece tratamento da obesidade baseado em mudanças de estilo de vida e acompanhamento multiprofissional, com acesso restrito a medicamentos. A sibutramina é prescrita em casos específicos, mas não está formalmente incluída na Relação Nacional de Medicamentos Essenciais (RENAME). Medicamentos mais recentes e eficazes, como semaglutida, liraglutida (Saxenda), tirzepatida (Mounjaro) e naltrexona/bupropiona (Contrave), ainda não foram incorporados ao SUS, limitando seu uso à rede privada. Essa situação reforça a necessidade de ampliar as opções terapêuticas no sistema público diante do aumento da prevalência da obesidade no país.
Essas diferenças regulatórias evidenciam a complexidade do equilíbrio entre inovação, segurança e sustentabilidade econômica no tratamento farmacológico da obesidade.
Barreiras Econômicas e Desafios na Comercialização: Acesso e Sustentabilidade
Apesar dos avanços importantes, o acesso a medicamentos para obesidade ainda enfrenta grandes obstáculos, especialmente devido ao alto custo de tratamentos como semaglutida e tirzepatida, o que limita seu uso em países com sistemas públicos de saúde subfinanciados, como o Brasil. Além do preço, a adesão ao tratamento é comprometida pelos efeitos colaterais gastrointestinais comuns aos agonistas de GLP-1 (náuseas, diarreia, constipação, dor abdominal) e similares observados na tirzepatida e na combinação de naltrexona/bupropiona. Esses efeitos, aliados ao custo, levam muitos pacientes a interromperem o uso.
No Brasil, a venda desses medicamentos é controlada, exigindo receita médica com retenção nas farmácias, para garantir o uso seguro e acompanhamento médico contínuo. Outro fator que dificulta o tratamento é o estigma social persistente em torno da obesidade, ainda vista como escolha pessoal, o que pode desmotivar pacientes e afetar a qualidade do atendimento.
Perspectivas Futuras: Inovação e Acesso Sustentável
O futuro da farmacoterapia para obesidade é promissor, com o desenvolvimento de agonistas triplos que combinam ações em GLP-1, GIP e glucagon, além de novas tecnologias para liberação de fármacos, como sistemas injetáveis de longa duração e formulações orais que podem melhorar a adesão.
Espera-se que agências reguladoras como FDA, EMA e ANVISA adotem processos mais rápidos e flexíveis para aprovação de medicamentos que apresentem benefícios claros. Modelos inovadores de precificação, como acordos de compartilhamento de risco e pagamentos por resultados, podem ampliar o acesso tanto no sistema público quanto na iniciativa privada.
Entretanto, o equilíbrio entre inovação, segurança, eficácia, custo e acessibilidade continuará sendo um desafio. A colaboração entre pesquisadores, indústria e reguladores será essencial para transformar avanços científicos em tratamentos acessíveis.
Por fim, políticas públicas precisam evoluir para reconhecer a obesidade como uma doença crônica que requer terapias contínuas, integrando prevenção e tratamento para reduzir também as comorbidades associadas, como diabetes tipo 2 e doenças cardiovasculares. A regulação eficiente e a promoção da equidade são cruciais para o sucesso do manejo da obesidade no cenário global.
Referências consultadas
Cheang JY, Moyle PM. Glucagon-Like Peptide-1 (GLP-1)-Based Therapeutics: Current Status and Future Opportunities beyond Type 2 Diabetes. ChemMedChem. 2018 Apr 6;13(7):662–71. doi:10.1002/cmdc.201700781.
Drucker DJ. GLP-1-based therapies for diabetes, obesity and beyond. Nat Rev Drug Discov. 2025 Apr 25. doi:10.1038/s41573-025-01183-8.
Agência Nacional de Vigilância Sanitária (ANVISA). Resolução RDC nº 50, de 21 de fevereiro de 2014. Diário Oficial da União. 2014. Disponível em:https://anvisalegis.datalegis.net/action/ActionDatalegis.php?acao=abrirTextoAto&cod_menu=8542&cod_modulo=310&link=S&numeroAto=00000050&orgao=RDC%2FDC%2FANVISA%2FMS&seqAto=000&tipo=RDC&valorAno=2014
Fieldhouse R. Obesity drugs made in China could power next wave of treatments. Nature News. 2025 Jun 30. Disponível em: https://www.nature.com/articles/d41586-025-01987-z.
European Medicines Agency. Guideline on clinical evaluation of medicinal products used in weight control. London: EMA; 2016. Disponível em: https://www.ema.europa.eu/en/clinical-evaluation-medicinal-products-used-weight-control-scientific-guideline
Food and Drug Administration. Guidance for industry: developing products for weight management. Silver Spring: FDA; 2007. Disponível em: https://www.fda.gov/media/71252/download.
Aronne LJ, Horn DB, le Roux CW, Ho W, Falcon BL, Gomez Valderas E, et al. Tirzepatide as Compared with Semaglutide for the Treatment of Obesity. N Engl J Med. 2025 Jul 3;393(1):26–36. doi:10.1056/NEJMoa2416394.
Endereço
Av. Luiz Boiteaux Piazza, 1302 - Sapiens Parque, Cachoeira do Bom Jesus, Florianópolis, Santa Catarina, Brasil.
Segunda a sexta-feira das 08:00 às 17:00 horas.
©2024 - Centro de Inovação e Ensaios Pré-Clínicos
Mapa do site
Serviços
+55 (48) 3332-8400
contato@cienp.org.br
